科研進展
我所葛紀(jì)彎團隊、舒躍龍團隊聯(lián)合中山大學(xué)團隊合作發(fā)現(xiàn)神經(jīng)氨酸酶廣譜抗流感抗體:為廣譜流感疫苗設(shè)計提供新思路
2025年8月2日,中山大學(xué)公共衛(wèi)生學(xué)院(深圳)陳耀慶教授團隊與我所葛紀(jì)彎團隊、舒躍龍團隊及香港大學(xué)袁碩峰團隊合作在Nature communications發(fā)表“Broad Neuraminidase Antibodies Confer Protection Against Seasonal and Avian Influenza Viruses”的研究成果。
研究團隊利用單B細(xì)胞高通量抗體篩選平臺,從流感感染者體內(nèi)分離出兩株廣譜性人源單抗CAV-F6和CAV-F34。這兩株抗體能高效結(jié)合數(shù)十年來流行的甲型流感(Group 1/2)和乙型流感病毒的神經(jīng)氨酸酶(NA),并顯著抑制多種NA亞型的酶活性,同時對近年流行的禽流感毒株也表現(xiàn)出強中和活性。在動物模型中,兩株抗體對季節(jié)性流感(A/California/04/2009(H1N1)、A/Guizhou/54/1989(H3N2))的預(yù)防或治療均實現(xiàn)100%保護;對H7N9(A/Anhui/1/2013 (H7N9) NIBRG-268)禽流感具有顯著防護效果,且CAV-F6(20 mg/kg)對奶牛源H5N1的預(yù)防保護率達100%。
研究團隊通過冷凍電鏡解析了抗體與四種NA抗原的復(fù)合物結(jié)構(gòu),闡明了其廣譜中和機制。(1)催化口袋阻斷:CAV-F6和CAV-F34的HCDR3像“鑰匙”插入NA活性中心,直接抑制酶活,并與保守殘基(R118、D151等)形成氫鍵網(wǎng)絡(luò);(2)結(jié)合模式差異:兩株抗體雖使用相同胚系基因(IGHV3-48/IGKV3-20),但結(jié)合角度不同;(3)表位高度保守:識別位點在1968-2025年間流行的H1N1/H5N1/H3N2毒株中高度保守;(4)關(guān)鍵殘基作用:R54與口袋外圍強相互作用,其突變(R54S)使抗體解離速率增加13倍,結(jié)合力顯著降低。該研究揭示了靶向NA活性中心的抗體廣譜機制,為通用流感疫苗設(shè)計提供了理論依據(jù)和候選分子。
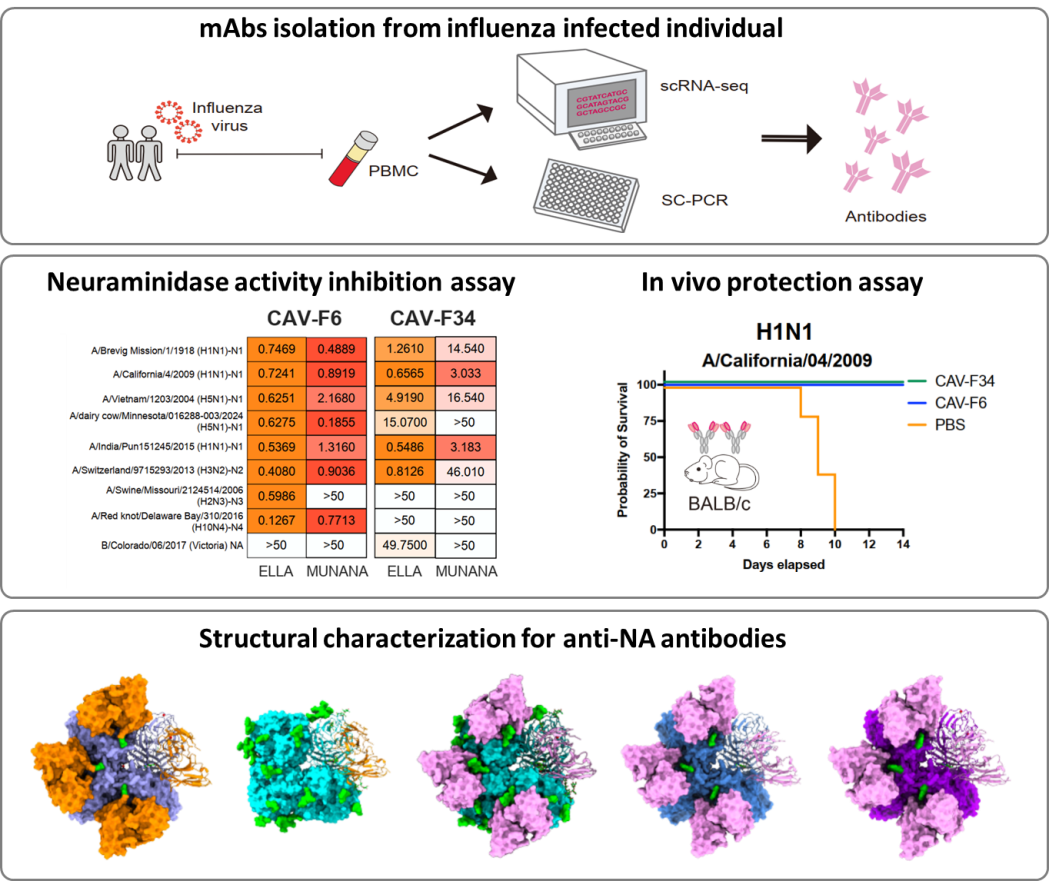
圖.針對流感病毒NA廣譜中和抗體的發(fā)現(xiàn)及評價示意圖
研究獲得了國家科技部重點研發(fā)項目(2021YFC2300100,2022YFC2304204)、深圳醫(yī)科院基金(B2302044)、深圳市科技計劃(RCJC20210706092009004、KQTD20200820145822023、ZDSYS20230626091203007、JCYJ2020010914243811),中國醫(yī)學(xué)科學(xué)院中央級公益性科研院所基本科研業(yè)務(wù)費專項資金項目(2023-RC180-01、2023-PT330-01),中國醫(yī)學(xué)科學(xué)院醫(yī)學(xué)與健康科技創(chuàng)新工程(2022-I2M-1-021),國家自然科學(xué)基金(32171202)等項目的支持。中山大學(xué)公共衛(wèi)生學(xué)院(深圳)陳耀慶教授,中國醫(yī)學(xué)科學(xué)院病原生物學(xué)研究所葛紀(jì)彎助理教授、舒躍龍教授,香港大學(xué)袁碩峰教授為共同通訊作者。中山大學(xué)公共衛(wèi)生學(xué)院呂可歆,清華大學(xué)生命學(xué)院李小曼,中山大學(xué)公共衛(wèi)生學(xué)院朱星晨、劉舒寧,香港大學(xué)微生物系蔡建飄為并列第一作者。清華大學(xué)王新泉教授參與了本研究并提供了重要幫助。
